Farmaco intelligente-immagine credit. public domain.
I farmaci intelligenti multi-target stanno rimodellando le terapie moderne, affrontando i complessi e interconnessi meccanismi che causano malattie come l’Alzheimer, il cancro e il disturbo depressivo maggiore. I progressi nell’intelligenza artificiale, nella modellistica molecolare e nella farmacologia di rete ne stanno accelerando lo sviluppo e migliorando la precisione terapeutica.
I farmaci tradizionali a bersaglio singolo, pur essendo precisi, hanno una capacità limitata di affrontare le complesse reti biologiche alla base delle malattie croniche e di prevenire la resistenza. Per superare queste problematiche e migliorare l’efficacia del trattamento, i farmaci intelligenti in grado di modulare simultaneamente diversi percorsi offrono un approccio a livello di sistema che si allinea alla natura multifattoriale di malattie come l’Alzheimer, il cancro e il disturbo depressivo maggiore.
Cosa sono i farmaci intelligenti intelligenti?
I farmaci intelligenti o multi-target sono agenti terapeutici rivoluzionari che regolano contemporaneamente numerosi recettori e cascate di segnalazione. Questo approccio di progettazione di farmaci multi-target (MTDD) sta rapidamente rimodellando la farmacologia moderna, grazie ai progressi nell’intelligenza artificiale (IA), nella modellistica molecolare e nella biologia dei sistemi.
Il docking molecolare assistito dall’intelligenza artificiale e lo screening virtuale prevedono come i composti interagiscono contemporaneamente con diversi target, mentre la modellazione farmacoforica identifica motivi strutturali condivisi che consentono il legame multirecettore. La farmacologia di rete mappa le complesse relazioni tra farmaci, target e circuiti patologici per identificare interazioni sinergiche. Nel frattempo, gli algoritmi di ottimizzazione multiobiettivo bilanciano potenza, selettività e proprietà farmacocinetiche, un flusso di lavoro sempre più adottato nelle pipeline di scoperta di farmaci in fase iniziale.
Attraverso la chemioinformatica e l’integrazione dei big data, i ricercatori estraggono vasti set di dati molecolari e clinici per identificare nuovi scaffold o modi in cui i farmaci esistenti potrebbero essere riutilizzati. Insieme, questi strumenti stanno semplificando la scoperta precoce dei farmaci, riducendo i fallimenti sperimentali grazie all’integrazione di dati omici, biomarcatori derivati dai pazienti e modelli predittivi basati sull’intelligenza artificiale.
Perché gli approcci multi-target sono importanti
Le MTDD superano i limiti degli interventi mono-bersaglio, affrontando la natura multifattoriale e adattiva di molte patologie. Coordinando gli effetti attraverso meccanismi biologici interconnessi, le MTDD amplificano il beneficio terapeutico e riducono la probabilità di resistenza ai farmaci, due importanti ostacoli nella gestione delle patologie neurodegenerative e oncologiche.
Malattia di Alzheimer
Nonostante decenni di ricerca, gli approcci farmacologici anti-amiloide hanno prodotto benefici limitati. Nuovi inibitori duali che prendono di mira la glicogeno sintasi chinasi-3 beta (GSK-3β) e la proteina tau, insieme ai modulatori dell’enzima β-site amiloid precursor protein cleaving enzyme 1 (BACE-1), si mostrano promettenti nel rallentare la progressione della malattia, soprattutto alla luce delle recenti evidenze che evidenziano la necessità di modulare simultaneamente l’amiloide, la proteina tau, lo stress ossidativo e le vie neuroinfiammatorie.
Composti come gli ibridi deossivasicinone-donepezil e i cannabinoidi di origine naturale, tra cui l’acido cannabidiolico (CBDA) e l’acido cannabigerolico (CBGA), mostrano anche attività multi-target attraverso i percorsi della colinesterasi e dell’amiloide ; tuttavia, le prove attuali rimangono in gran parte precliniche e in vitro, sottolineando la necessità di studi traslazionali.
Disturbo depressivo maggiore (MDD)
Il disturbo depressivo maggiore deriva da alterazioni nelle interazioni tra i sistemi della serotonina e del glutammato che regolano l’umore, la cognizione e la neuroplasticità. I tradizionali inibitori selettivi della ricaptazione della serotonina (SSRI), che agiscono sui trasportatori della serotonina, spesso producono risposte ritardate o parziali. Al contrario, gli antidepressivi multimodali avanzati regolano diversi sistemi recettoriali contemporaneamente per ripristinare l’equilibrio neurochimico e ottimizzarne l’efficacia.
Il Vilazodone, attualmente approvato per l’uso negli Stati Uniti, combina l’inibizione della ricaptazione della serotonina con la stimolazione parziale del recettore 1A della 5-idrossitriptamina (5-HT1A) per rafforzare l’umore e le funzioni cognitive, limitando al contempo gli effetti collaterali indesiderati. Studi preclinici dimostrano che il Vilazodone produce un maggiore rilascio di serotonina e risposte simil-antidepressive più intense rispetto alla Paroxetina o alla Fluoxetina; tuttavia, dosi più elevate possono essere associate a lievi effetti gastrointestinali. La Vortioxetina agisce su cinque sottotipi di recettori della serotonina per esercitare effetti antidepressivi e pro-cognitivi attraverso la regolazione indiretta del glutammato, un effetto supportato da evidenze che mostrano una modulazione serotoninergica della plasticità sinaptica indotta dai recettori AMPA e NMD
Nuovi composti come destrometorfano-bupropione (Auvelity) ed sketamina agiscono contemporaneamente sulla neuroplasticità legata all’N-metil-D-aspartato (NMDA), alle monoammine e al fattore neurotrofico cerebrale (BDNF). Lo spray nasale di Esketamina, autorizzato dalla Food and Drug Administration (FDA) statunitense, offre un rapido sollievo dalla depressione recidivante, sebbene l’eterogeneità dei risultati degli studi di fase III sottolinei la necessità di una selezione dei pazienti basata sui biomarcatori.
Cancro
In oncologia, la recidiva rimane una preoccupazione importante, poiché contribuisce a quasi il 90% dei decessi correlati al cancro. I composti multi-azione bloccano la segnalazione compensatoria per aumentare i tassi di risposta, limitare la tolleranza e, in definitiva, migliorare gli esiti clinici per i pazienti.
Ad esempio, gli inibitori a doppio percorso che prendono di mira la fosfatidilinositolo 3-chinasi/bersaglio della rapamicina nei mammiferi (PI3K/mTOR) e la proteina chinasi attivata da mitogeni/fibrosarcoma rapidamente accelerata (RAF/MEK) prevengono la riattivazione del percorso, il che porta a risposte terapeutiche sostenute.
Nuovi farmaci come Imatinib e Sunitinib hanno aperto la strada a questo approccio inibendo simultaneamente più tirosin-chinasi, tra cui la regione del cluster di breakpoint-abelson (BCR-ABL), il proto-oncogene c-KIT e il recettore alfa del fattore di crescita derivato dalle piastrine (PDGFR). Questi farmaci hanno trasformato i risultati nella leucemia mieloide cronica (LMC), nei tumori stromali gastrointestinali (GIST) e nei tumori renali. Gli inibitori di seconda generazione, tra cui Pazopanib, Cabozantinib ed Entrectinib, aumentano ulteriormente la precisione e la penetrazione della barriera emato-encefalica (BBB), prolungando così la sopravvivenza, sottolineando il vantaggio di colpire più nodi all’interno delle reti di segnalazione oncogenica.
 Credito di immagine: Gorodenkoff/Shutterstock.com
Credito di immagine: Gorodenkoff/Shutterstock.com
Vantaggi
I farmaci basati su reti intelligenti offrono un approccio trasformativo per il trattamento di patologie biologicamente complesse, offrendo una copertura molecolare più ampia e una sinergia a livello di pathway all’interno di una singola molecola. A differenza degli agenti a bersaglio singolo, questi composti possono modulare simultaneamente diversi meccanismi biologici interdipendenti, producendo effetti additivi o sinergici che rafforzano le prestazioni cliniche complessive. Questa attività concertata consente dosaggi inferiori, riducendo al minimo la tossicità e mantenendone l’efficacia.
Nella malattia di Alzheimer, la MTDD migliora la penetrazione della barriera emato-encefalica, riduce la tossicità correlata al metabolismo e limita la politerapia. Progetti innovativi basati su chimere mirate alla proteolisi (PROTAC) che impiegano la chimica di legatura dei triazoli sono associati alla degradazione selettiva delle proteine tau patogene con maggiore permeabilità alla barriera emato-encefalica, sebbene gli attuali candidati PROTAC siano ancora in fase di sviluppo preclinico.
Allo stesso modo, le terapie basate sull’acido ribonucleico (RNA), come il piccolo RNA interferente (siRNA) coniugato a n-acetil-D-galattosamina (GalNAc) e i sistemi di rilascio di particelle lipidiche di acidi nucleici stabili (SNALP), hanno ottenuto un rilascio cerebrale efficiente e un robusto silenziamento delle trascrizioni rilevanti per la malattia nei modelli animali, ma la traduzione clinica rimane limitata.
Oltre alla neurodegenerazione, i ligandi multi-target (MTDL) in oncologia e malattie infettive riducono la tolleranza ai farmaci prendendo di mira più nodi all’interno delle reti di segnalazione adattiva. Nel complesso, queste strategie ampliano la finestra terapeutica, migliorando al contempo l’aderenza terapeutica del paziente, la sicurezza e la durata delle risposte terapeutiche.
Sfide
Nonostante il loro potenziale di trasformare la terapia, la progettazione di farmaci integrati intelligenti presenta notevoli sfide scientifiche, tecniche e normative. Progettare una singola molecola in grado di modulare reti diverse richiede una profonda conoscenza della biologia delle reti di malattie e delle interazioni tra bersagli.
Bilanciare l’ efficacia su più target senza indurre tossicità off-target rimane una sfida significativa. I composti multi-target possono interferire involontariamente con molecole biologiche non correlate, causando effetti avversi o esiti farmacologici imprevedibili.
L’ottimizzazione dei profili di assorbimento, distribuzione, metabolismo ed escrezione (ADME) per i farmaci che agiscono su siti diversi aumenta la complessità della progettazione di questi farmaci intelligenti, soprattutto perché le proprietà fisico-chimiche adatte a una classe target possono ostacolare le interazioni con un’altra.
Gli agenti multi-target richiedono inoltre una validazione preclinica più estesa, studi farmacocinetici integrati e studi clinici più lunghi per valutarne la sicurezza e le interazioni sistemiche. Nel complesso, questi fattori comportano costi di ricerca e sviluppo (R&S) più elevati e tassi di abbandono dovuti a tempi lunghi, alti tassi di fallimento e difficoltà tecniche nell’agire attraverso processi molecolari coordinati.
Nelle malattie neurodegenerative come l’AD, l’attraversamento della barriera emato-encefalica rappresenta una limitazione significativa, ulteriormente complicata dall’eterogeneità della patologia del paziente, che richiede strategie di prioritizzazione dei bersagli individualizzati. Tuttavia, i recenti progressi nella modellazione basata sull’intelligenza artificiale, nei sistemi di nanocarrier e nella prioritizzazione razionale dei bersagli hanno il potenziale per superare queste sfide.
Leggi anche: Nuovo farmaco intelligente promettente per il carcinoma mammario triplo negativo metastatico
Prospettive future
I progressi nella progettazione di farmaci basata sull’intelligenza artificiale e nell’integrazione di biomarcatori digitali stanno accelerando lo sviluppo di farmaci intelligenti multi-target. L’intelligenza artificiale può analizzare vasti set di dati biologici per identificare target sinergici, ottimizzare i composti guida e prevedere l’efficacia e la sicurezza clinica, riducendo i tempi di sviluppo e i fallimenti degli studi clinici, consentendo la simulazione in tempo reale delle risposte biologiche e l’ottimizzazione degli studi clinici basata su gemelli digitali.
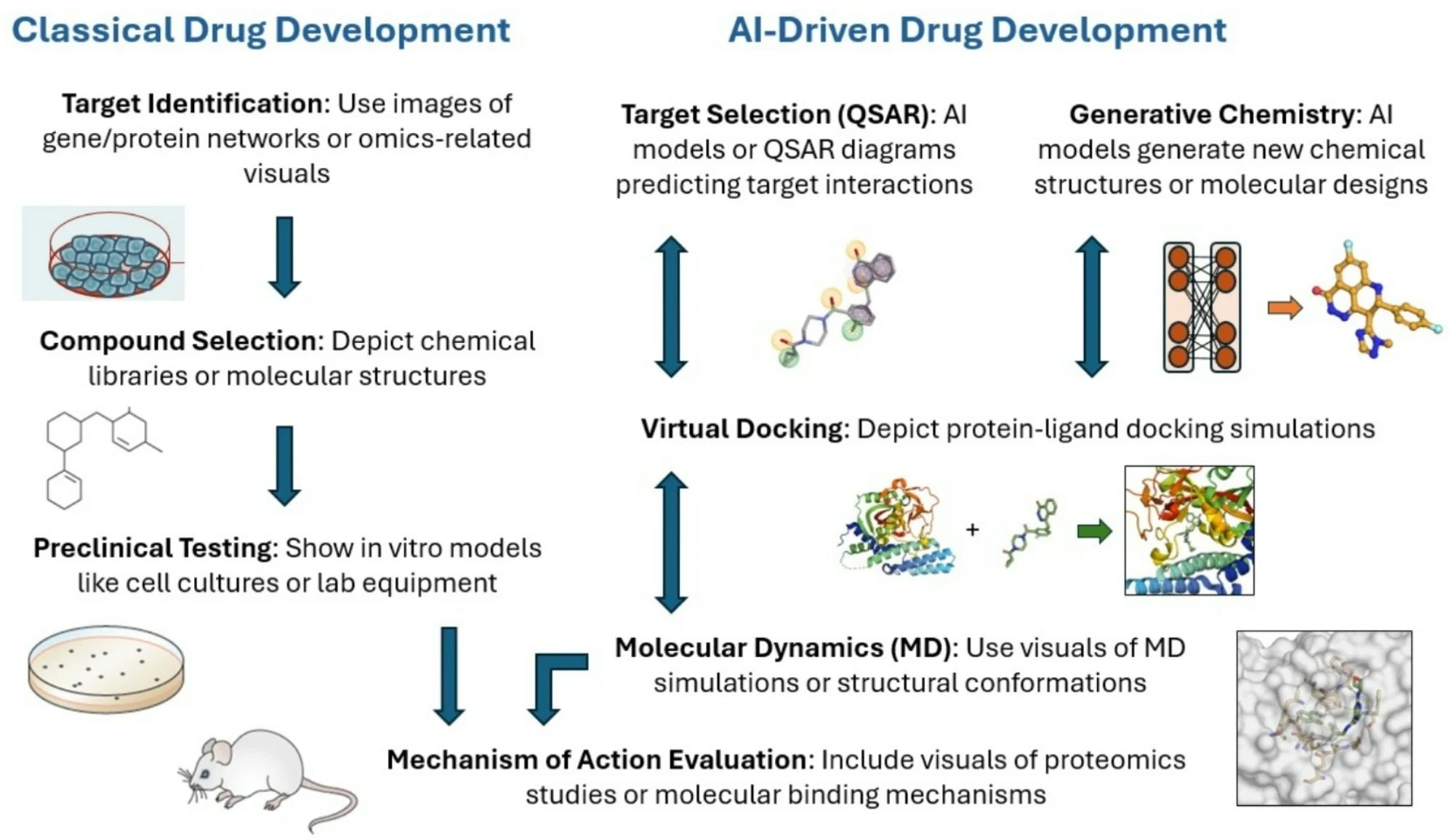
Descrizione dello sviluppo di farmaci classico rispetto a quello guidato dall’intelligenza artificiale
Allo stesso tempo, i biomarcatori digitali provenienti da dispositivi indossabili e sensori mobili facilitano il monitoraggio continuo e reale delle risposte terapeutiche, supportando strategie terapeutiche personalizzate. Insieme, queste innovazioni stanno rimodellando la scoperta di nuovi farmaci in un processo basato sui dati e incentrato sul paziente.
Fonte:Current Medical Chemistry