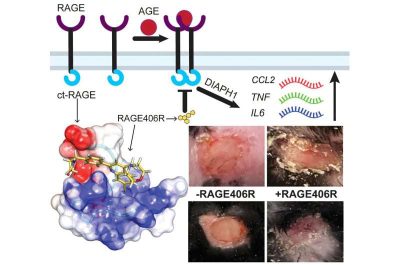
Diabete di tipo 1 e 2-immagine: abstract grafico. Crediti: Cell Chemical Biology (2025).
I ricercatori dell’Università di Albany e della NYU Grossman School of Medicine hanno scoperto un modo per bloccare un percorso cellulare chiave noto per causare infiammazione cronica e compromissione della guarigione delle ferite nelle persone affette da diabete tipo 1 e di tipo 2.
Questa scoperta potrebbe offrire una nuova opzione terapeutica per bloccare alla radice gli effetti dannosi del diabete di tipo 1 e di tipo 2.
Nel loro ultimo lavoro, i ricercatori hanno identificato con successo – e sviluppato un farmaco a piccole molecole per interrompere – una reazione a catena intracellulare che contribuisce in modo significativo alle complicanze indotte dal diabete. I loro risultati, sono stati pubblicati all’inizio di questo mese sulla copertina di Cell Chemical Biology.
“Gli attuali trattamenti per il diabete si concentrano principalmente sul rallentamento della progressione della malattia; tuttavia, non affrontano l’infiammazione di fondo che contribuisce alle complicazioni del diabete”, ha affermato Alexander Shekhtman, coautore senior e Professore presso il Dipartimento di Chimica e l’RNA Institute dell’Università di Albany. “I nostri risultati indicano un nuovo promettente percorso per il trattamento futuro del diabete. I risultati di questo studio serviranno da trampolino di lancio per lo sviluppo di terapie per entrambi i tipi di diabete e per la progettazione di marcatori in grado di misurare l’efficacia del nuovo trattamento negli animali vivi“.
Nel 2021, oltre 38 milioni di americani, ovvero oltre l’11% della popolazione, convivevano con il diabete. Gli attuali trattamenti possono aiutare i pazienti a gestire la glicemia, ma non esistono farmaci progettati per trattare l’infiammazione caratteristica della malattia, che provoca una serie di complicazioni patologiche in tutto l’organismo. La nuova piccola molecola del team, un composto chiamato RAGE406R, potrebbe rispondere a questa esigenza.
“RAGE406R agisce su un pathway molto importante che non comprendiamo ancora appieno”, ha affermato Shekhtman. “In futuro, ho intenzione di utilizzare una combinazione di approcci classici di biologia strutturale e molecolare, insieme alla nostra tecnica sviluppata internamente, la risonanza magnetica nucleare in-cell, per chiarire il meccanismo che regola questo pathway. Abbiamo inoltre intenzione di collaborare con un team clinico per supportare gli sforzi di sviluppo del farmaco e portare RAGE406R sul mercato“.
Come funziona RAGE406R
Nelle persone con diabete, un tipo di molecola dannosa chiamata “prodotti finali di glicazione avanzata” si accumula nei tessuti di tutto il corpo. Queste molecole attivano un sensore di superficie cellulare noto come “recettore per i prodotti finali di glicazione avanzata” (RAGE), che a sua volta innesca una struttura molecolare all’interno delle cellule chiamata “Diafano-1” (DIAPH1). Tipicamente, DIAPH1 supporta le normali funzioni cellulari, ma se sovrastimolata, porta a infiammazione cronica, causando problemi come malattie cardiovascolari e una lenta guarigione delle ferite.
Utilizzando tecniche di biologia strutturale, il team di ricerca ha costruito un modello per comprendere come il recettore RAGE attivi DIAPH1. Ciò ha permesso loro di individuare un sito di legame su DIAPH1 che facilita il percorso.
“Per questo progetto, ho analizzato più di 100 molecole diverse utilizzando la risonanza magnetica nucleare e la spettroscopia di fluorescenza per identificare la struttura molecolare più capace di legarsi e inibire un pathway che porta all’infiammazione nei pazienti diabetici. È così che siamo arrivati alla nostra molecola, RAGE406R“, ha spiegato il coautore principale Parastou Nazarian, dottorando al terzo anno presso il Dipartimento di Chimica dell’Università di Albany. “La nostra molecola agisce essenzialmente legandosi al sito del recettore RAGE che DIAPH1 occupa tipicamente. Bloccando questa connessione, la molecola blocca l’innesco dell’infiammazione. Credo che la struttura molecolare che abbiamo identificato, attraverso una combinazione di approcci chimici e biologici, mostri un forte potenziale per ridurre l’infiammazione cronica”.
Leggi anche:Non tutto il diabete è dovuto allo zucchero: capire il diabete insipido
Dimostrazione del potenziale di efficacia clinica
La molecola si è dimostrata efficace quando testata sia su cellule umane che su topi. RAGE406R ha ridotto significativamente i livelli di un importante messaggero infiammatorio nelle cellule umane prelevate da campioni di sangue di persone con diabete di tipo 1. Le molecole hanno anche accelerato la guarigione delle ferite e ridotto la risposta infiammatoria nei topi con diabete di tipo 2.
Questi risultati confermano che RAGE406R potrebbe rappresentare un modo per controllare le complicanze croniche del diabete, fornendo al contempo biomarcatori specifici per monitorare l’efficacia del farmaco in futuri studi clinici.
“Attualmente non esistono trattamenti che affrontino le cause profonde delle complicazioni diabetiche e il nostro lavoro dimostra che RAGE406R può farlo, non abbassando i livelli elevati di zucchero nel sangue, ma bloccando l’azione intracellulare di RAGE“, ha affermato la co-autrice senior, la Dott.ssa Ann Marie Schmidt, Professoressa di Endocrinologia Dr. Iven Young presso la NYU Grossman School of Medicine.
“Se confermato da ulteriori test condotti su soggetti umani, il composto potrebbe potenzialmente colmare le lacune nel trattamento, tra cui il fatto che la maggior parte dei farmaci attuali funziona solo contro il diabete di tipo 2“.
Fonte: Cell Chemical Biology