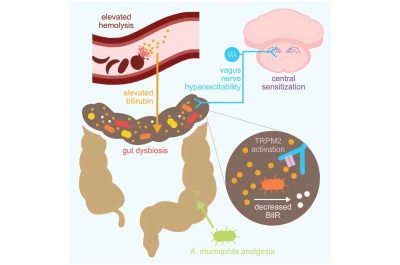
Anemia falciforme-immagine abstract grafico. Crediti: Cell Host & Microbe
Una collaborazione di ricerca che ha coinvolto scienziati e studenti dell’Università del Texas a Dallas ha scoperto una chiara correlazione tra il dolore cronico causato dall’anemia falciforme e dai batteri presenti nel tratto gastrointestinale.
La Dott.ssa Katelyn Sadler, Prof.ssa associata di neuroscienze presso la Facoltà di Scienze comportamentali e cerebrali, è l’autrice corrispondente dello studio condotto su topi e tessuti umani e pubblicato online il 16 settembre sulla rivista Cell Host & Microbe.
I ricercatori dell’Università del Texas a Dallas e del Medical College of Wisconsin (MCW) si sono concentrati sull’Akkermansia muciniphila, un batterio comunemente presente nell’intestino umano, ma notoriamente meno diffuso negli individui affetti da anemia falciforme. Nello studio, il team ha alleviato il dolore cronico in topi geneticamente modificati per essere affetti da anemia falciforme trapiantando batteri dalle feci di topi sani nel tratto digerente degli animali affetti da anemia falciforme.
“I nostri risultati sono una forte prova che il contenuto del microbioma negli individui affetti da anemia falciforme potrebbe causare dolore cronico“, ha affermato Sadler.
L’anemia falciforme è una malattia genetica in cui i globuli rossi assumono una forma anomala, simile a quella di una falce, e diventano rigidi. Gli individui affetti da anemia falciforme possono provare un dolore improvviso e acuto a causa delle cellule deformi che bloccano il flusso sanguigno e privano di ossigeno alcune aree del corpo. Per ragioni non chiare, almeno il 50% degli individui affetti da anemia falciforme soffre anche di dolore cronico.
“I due tipi di dolore hanno patologie distinte”, ha affermato Sadler, “e si ritiene che il microbioma intestinale svolga un ruolo nel dolore cronico”.
“I batteri e altri composti presenti nell’apparato digerente hanno effetti diversi e pervasivi che vanno oltre quanto ci si possa aspettare“, ha affermato. “Il sistema immunitario può attivarsi maggiormente grazie ai batteri intestinali e questo può avere implicazioni di vasta portata per l’organismo. L’idea che il microbioma intestinale sia la causa del dolore cronico in altre parti del corpo sta diventando sempre più diffusa, come dimostrano anche recenti ricerche sulla fibromialgia“.
L’A. muciniphila è disponibile senza ricetta medica come integratore probiotico. Sadler ha affermato che lo studio del gruppo è il primo a identificare il batterio come bersaglio per il dolore associato all’anemia falciforme.
“Abbiamo identificato l’Akkermansia perché produce acidi grassi a catena corta, che sembrano cruciali per alleviare il dolore”, ha affermato Sadler. “Trapiantandolo nei nostri topi affetti da anemia falciforme, il loro dolore cronico è quasi completamente regredito. È interessante notare che, quando abbiamo trapiantato tutti i batteri dai topi affetti da anemia falciforme ad animali senza anemia falciforme, abbiamo trasferito anche il dolore: non la malattia genetica del sangue, ma l’ ipersensibilità al tatto e al freddo .”
Sadler ha affermato che modificando il contenuto dell’intestino si possono attivare le terminazioni nervose nell’intestino che inviano segnali al sistema nervoso centrale.
“Ciò che pensiamo accada specificamente in questi esperimenti sull’anemia falciforme è una sensibilizzazione centrale“, ha affermato. “Tutto diventa più sensibile a causa di un cambiamento nel cervello o nel midollo spinale“.
Il microbioma intestinale umano è in continua evoluzione, non solo nel breve termine a causa delle fluttuazioni quotidiane della dieta, ma anche nel lungo termine in relazione a fattori quali età, stile di vita, farmaci e ambiente.
“I probiotici come l’Akkermansia possono essere molto utili alla luce di questa frequente evoluzione“, ha affermato Sadler, “anche se crediamo che prima o poi si dovrà cambiare probiotico, poiché i batteri nell’intestino si adattano per uccidere l’Akkermansia“.
L’autrice principale dello studio è la Dott.ssa Amanda Brandow, Prof.ssa di pediatria ed ematologa presso il MCW, che cura i bambini con dolore associato all’anemia falciforme. Lei e Sadler collaborano dal 2017.
“Il dolore cronico causato dall’anemia falciforme ha un profondo impatto negativo sulla qualità della vita delle persone affette dalla malattia”, ha affermato Brandow. “Questi risultati sono estremamente entusiasmanti, poiché forniscono dati preclinici a supporto di una sperimentazione clinica che utilizza probiotici o il trapianto di microbiota fecale come nuovo trattamento per il dolore cronico causato dall’anemia falciforme“.
Sadler ha descritto il potenziale sviluppo di un farmaco terapeutico per il dolore cronico da anemia falciforme come “una soluzione che cambierà la vita“.
“Questi pazienti non hanno molte opzioni per la gestione dei sintomi al momento”, ha affermato. “La terapia genica è una novità e ha un costo proibitivo per la maggior parte delle persone e i pazienti che la ricevono devono sottoporsi a chemioterapia. Anche in questo caso, nei nuovi studi sulla terapia genica, non è stato valutato il dolore cronico, ma solo quello acuto. Questa idea è un tipo di terapia che non è mai stata esplorata prima. Potrebbe essere relativamente poco costosa per le persone che, al momento, vengono spesso respinte quando cercano farmaci antidolorifici”.
La Dott.ssa Kelli Palmer, autrice dello studio e Prof.ssa di scienze biologiche presso l’Università del Texas a Dallas, ha chiesto ai suoi studenti di coltivare i batteri A. muciniphila necessari per lo studio, utilizzando un’incubatrice anaerobica, che coltiva le cellule in un ambiente a basso contenuto di ossigeno.
Leggi anche:Anemia falciforme: potenziale strategia terapeutica potrebbe prevenire le complicazioni
Spiegano gli autori:
“In questo studio, abbiamo identificato specifici batteri intestinali e metaboliti dell’ospite che causano il dolore cronico da SCD. Nello specifico, abbiamo determinato che il contenuto del tratto gastrointestinale di topi SCD, quando trapiantato in un animale altrimenti inesperto, induce un dolore diffuso che rispecchia da vicino i comportamenti dolorosi manifestati dai donatori fecali di SCD. Questo dolore è indotto dalla segnalazione della bilirubina attraverso i canali TRPM2. La bilirubina, un prodotto di degradazione dell’eme catabolizzato dai batteri intestinali, attiva direttamente e aumenta l’eccitabilità degli afferenti vagali, portando alla sensibilizzazione centrale. Analogamente, il trapianto di un microbiota intestinale sano in topi SCD allevia temporaneamente il dolore cronico negli animali riceventi. Questo effetto analgesico deriva, in parte, dalla maggiore abbondanza di Akkermansia muciniphila nell’ambiente gastrointestinale. L’integrazione con il probiotico A. muciniphila ha invertito il dolore cronico nei topi SCD, ma non attraverso meccanismi canonici. L’identificazione della bilirubina gastrointestinale come fattore primario del dolore cronico da SCD è una scoperta innovativa associata a numerose opportunità terapeutiche”.
“Abbiamo reclutato un team di studenti magistrali del mio corso di laurea in biochimica per fare brainstorming su esperimenti su come il microbioma intestinale influisce sul dolore“, ha affermato Palmer, titolare della cattedra Cecil H. e Ida Green in Biologia dei Sistemi presso la Facoltà di Scienze Naturali e Matematica. “Abbiamo chiesto agli studenti dei nostri corsi di laurea magistrale di svolgere il lavoro sull’Akkermansia nel mio laboratorio, creando questa opportunità per gli studenti di biologia di dedicarsi a ricerche interdisciplinari”.
Fonte: Cell Host & Microbe