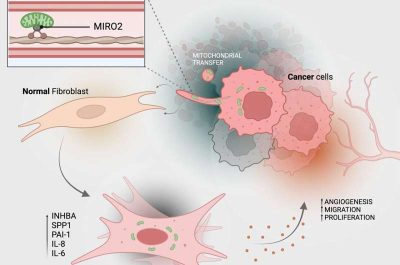
Cancro-immagine: ecco come le cellule tumorali trasferiscono i loro mitocondri (in verde) alle cellule del tessuto connettivo (fibroblasti). Crediti: Michael Cangkrama / ETH Zurigo / BioRender
Le cellule tumorali forniscono alle cellule sane vicine ulteriori mitocondri per consentirle di lavorare. Questo è stato dimostrato dai ricercatori del Politecnico federale di Zurigo in un nuovo studio. In questo modo, il cancro sfrutta un meccanismo che spesso serve a riparare le cellule danneggiate.
I tumori hanno sviluppato numerose strategie e trucchi per ottenere vantaggi dall’organismo. Guidati dalla Prof.ssa di biologia cellulare Sabine Werner, i ricercatori del Politecnico federale di Zurigo hanno ora scoperto un altro sorprendente trucco a cui alcuni tumori ricorrono per garantire la propria sopravvivenza e crescita.
In uno studio pubblicato sulla rivista Nature Cancer, i biologi dimostrano che le cellule tumorali della pelle sono in grado di trasferire i loro mitocondri alle cellule sane del tessuto connettivo (fibroblasti) nelle loro immediate vicinanze. I mitocondri sono i compartimenti cellulari che forniscono energia sotto forma di molecola di ATP.
Le cellule cancerose utilizzano minuscoli tubi costituiti da materiale di membrana cellulare per trasferire i mitocondri e collegare le due cellule, un po’ come in un sistema di tubi pneumatici.
Riprogrammazione funzionale
Il trasferimento mitocondriale riprogramma funzionalmente i fibroblasti trasformandoli in fibroblasti associati al tumore, che supportano principalmente le cellule tumorali: i fibroblasti associati al tumore si moltiplicano solitamente più velocemente dei fibroblasti normali e producono più ATP, secernendo anche maggiori quantità di fattori di crescita e citochine. E tutto questo va a vantaggio delle cellule tumorali: si moltiplicano anche più velocemente, rendendo il tumore più aggressivo.
Infine, ma non meno importante, i fibroblasti sequestrati alterano anche l’ambiente cellulare, la cosiddetta matrice extracellulare, aumentando la produzione di alcuni componenti della matrice, favorendo la proliferazione delle cellule tumorali. La matrice extracellulare è vitale per la stabilità meccanica dei tessuti e influenza la crescita, la guarigione delle ferite e la comunicazione intercellulare.
Da scoperta casuale a terapia?
“In realtà, si è trattato di una scoperta casuale”, come ha raccontato Sabine Werner. Il suo ex ricercatore post-dottorato, Michael Cangkrama, ha scoperto minuscole connessioni tubolari tra i due tipi di cellule in una capsula di Petri contenente una co-coltura di fibroblasti e cellule tumorali della pelle. È stato quindi in grado di dimostrare che i mitocondri delle cellule tumorali vengono trasferiti nei fibroblasti attraverso queste nano-connessioni.
Il fatto che le cellule siano in grado di scambiare mitocondri attraverso queste connessioni non è di per sé una novità. Ad esempio, diversi anni fa gli scienziati hanno scoperto che dopo un ictus, le cellule sane del tessuto nervoso trasmettono i loro organelli energetici alle cellule nervose danneggiate per garantirne la sopravvivenza.
“Le cellule tumorali sfruttano in realtà un meccanismo per i propri scopi, che si rivela utile in caso di lesione. Questo permette loro di trasformarsi in tumori maligni“, spiega Werner.
Altri gruppi di ricerca hanno dimostrato che le cellule provenienti dall’ambiente tumorale possono trasferire i propri mitocondri alle cellule tumorali, migliorando così l’idoneità delle cellule tumorali riceventi. Finora, tuttavia, non si sapeva che il trasferimento mitocondriale funziona anche al contrario, dalle cellule tumorali della pelle alle cellule sane del tessuto connettivo.
In collaborazione con altri gruppi di ricerca del Politecnico Federale di Zurigo, i ricercatori hanno trovato prove che questo trasferimento gioca un ruolo anche in altri tipi di cancro, come il cancro al seno e il cancro al pancreas. Ciò è particolarmente importante in quest’ultimo caso, perché i tumori del pancreas contengono molti fibroblasti e il loro tessuto connettivo è relativamente grande.
La proteina MIRO2 aiuta nel trasferimento
Infine, i ricercatori hanno anche chiarito il meccanismo molecolare alla base del trasferimento mitocondriale. Era già noto che alcune proteine contribuissero al trasporto dei mitocondri. I ricercatori hanno studiato quali di queste proteine fossero presenti in gran numero nelle cellule tumorali che trasferiscono i mitocondri e hanno scoperto la proteina MIRO2.
“Questa proteina viene prodotta in quantità molto elevate nelle cellule tumorali che trasferiscono i loro mitocondri“, afferma Werner.
Leggi anche:Acido laurico, composto chiave nella lotta contro il cancro
I ricercatori hanno rilevato MIRO2 non solo nelle colture cellulari, ma anche in campioni di tessuto umano, in particolare nelle cellule tumorali ai margini dei tumori che crescono in modo invasivo nel tessuto e si presentano in stretta prossimità dei fibroblasti.
“Siamo riusciti a rilevare MIRO2 esattamente dove ci aspettavamo che fosse”, ha affermato il primo autore Michael Cangkrama.
Spiegano gli autori:
“I mitocondri sono fondamentali per la conversione energetica e gli eventi di segnalazione e sono coinvolti nelle decisioni sul metabolismo e sul destino cellulare in condizioni di salute e malattia. Un tempo specie alfaproteobatterica evolutasi in un organello, i mitocondri persistono come unità funzionalmente specializzate, dotate della capacità di muoversi tra le cellule. Questo fenomeno, noto come trasferimento mitocondriale, è emerso come una potente strategia per la rivitalizzazione e il ringiovanimento dei tessuti in organi danneggiati o malati. Studi recenti hanno identificato ruoli importanti della dinamica mitocondriale nel cancro, rivelando come il trasferimento mitocondriale contribuisca all’eterogeneità metabolica tra le cellule tumorali e influenzi gli esiti della malattia e le risposte al trattamento. Il trasferimento mitocondriale può avvenire attraverso giunzioni comunicanti, vescicole extracellulari, rilascio e assorbimento mitocondriale diretto o nanotubi tunnel (TNT), che sono sottili strutture membranose che formano connessioni dinamiche tra le cellule. È stato anche segnalato il trasferimento di mitocondri dalle cellule stromali o immunitarie nel microambiente tumorale alle cellule tumorali, che ha promosso la crescita tumorale. Ad esempio, il trasferimento mitocondriale da cellule T CD8 + , cellule staminali mesenchimali o fibroblasti associati al cancro (CAF) alle cellule tumorali è stato descritto per diversi tumori, con conseguente aumento della proliferazione, della motilità e del metabolismo del lattato delle cellule tumorali. Tuttavia, il processo opposto – il trasferimento mitocondriale dalle cellule tumorali alle cellule stromali, inclusi i fibroblasti – non è stato segnalato, sebbene ciò possa avere importanti conseguenze per il fenotipo dei fibroblasti. In questo studio, identifichiamo il trasferimento mitocondriale dalle cellule tumorali ai fibroblasti come un regolatore chiave della differenziazione dei CAF“.
Alla ricerca di un inibitore
Le nuove scoperte offrono spunti per arrestare la crescita tumorale. Quando i ricercatori hanno bloccato la formazione di MIRO2, il trasferimento mitocondriale è stato inibito e i fibroblasti non si sono sviluppati in fibroblasti promotori del tumore .
“Il blocco di MIRO2 ha funzionato in provetta e nei modelli murini. Resta da vedere se funziona anche nei tessuti umani“, afferma Werner. Per scoprirlo, i ricercatori devono prima identificare un inibitore di MIRO2 che abbia pochi effetti collaterali nell’organismo umano.
“Se avrà successo, un simile inibitore potrebbe essere trasferito ad applicazioni cliniche a lungo termine Tuttavia, è probabile che ci vorranno anni prima che una terapia del genere venga sviluppata e testata“, dice Werner.
Fonte:Nature Cancer