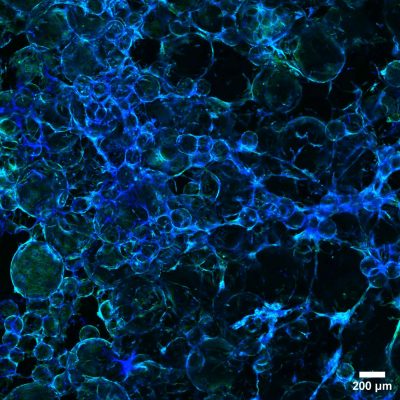
Carne sostenibile-Immagine: ecco come appare la carne coltivata in laboratorio al microscopio. Foto credito: Aman Chahal e Angelica Rossi, SINTEF.
In questo laboratorio i ricercatori stanno coltivando il cibo del futuro: carne realizzata utilizzando le alghe come alternativa agli ingredienti di origine animale.
È possibile coltivare carne in laboratorio. E poi si può preparare un hamburger senza dover macellare un toro o una mucca. Ma al momento è ancora incredibilmente costoso.
La carne coltivata in laboratorio, o coltivata in vitro, richiede molto spazio. Spesso il sangue di vitelli abortiti e microsfere non commestibili di dimensioni microscopiche sono ingredienti necessari. La situazione cambierà se la ricercatrice senior Hanna Haslene-Hox e i suoi colleghi dell’istituto scientifico norvegese SINTEF raggiungeranno il loro obiettivo.
Creare proteine animali – senza animali
“Come possiamo produrre proteine animali senza coinvolgere affatto gli animali, o in misura molto minore?“. È così che Haslene-Hox delinea la grande questione su cui SINTEF e Nofima stanno lavorando insieme.
A tal fine, i ricercatori hanno utilizzato alghe marine, il sottogruppo più numeroso di alghe, oltre ad altre specie di alghe e residui vegetali, al posto di sangue e materiale sintetico.
Perché queste proteine diventino cibo per l’uomo, produrle in laboratorio non è sufficiente. Bisogna coltivarle su larga scala e a costi più bassi.
“Il primo hamburger prodotto in laboratorio è stato prodotto nel 2013. È costato 250.000 euro“, racconta Haslene-Hox.
Necessità di una cultura delle sospensioni più efficiente
Le cellule muscolari che i ricercatori norvegesi stanno coltivando devono attaccarsi a qualcosa nella coltura in sospensione.
“Lo facciamo molto bene in bottiglie di coltura, dove le cellule possono crescere in uno strato sottilissimo sulla plastica. Ma per coltivare abbastanza cellule per un chilo di carne in questo modo, ci vorrebbero 700 metri quadrati di bottiglie. Non è molto pratico“, dice Haslene-Hox. Settecento metri quadrati equivalgono a dieci appartamenti norvegesi di medie dimensioni.
La chiave è uno strato più spesso
Le cellule crescono in uno strato spesso meno di un centesimo di millimetro. Affinché la carne coltivata in laboratorio diventi comune, i ricercatori devono prima consentire alle cellule di crescere verso l’alto.
“Invece di crescere solo su una superficie piana, potrebbero crescere su minuscole microsfere portanti. Poi potremmo riempire un serbatoio con microsfere contenenti cellule. In questo modo si crea una superficie molto più ampia su cui le cellule possono crescere“, afferma il ricercatore senior.
Questo approccio è già in una certa misura utilizzato oggi. I ricercatori utilizzano, ad esempio, microcarrier sferici realizzati in destrano. Il destrano è una lunga catena di molecole di zucchero chiamata polisaccaride.
Dai materiali sintetici alle alghe commestibili
“Ma non si possono mangiare queste perle non commestibili. Quello che bisogna fare se si vuole preparare una bistecca o un hamburger è staccare le cellule dai microcarrier dopo che sono cresciute a sufficienza. È un’operazione che richiede molte risorse e molte cellule non la tollerano, quindi muoiono durante il trattamento. Questo genera molti rifiuti nel processo“, afferma Haslene-Hox.
Ciò che SINTEF e Nofima cercano di realizzare è utilizzare materiali di origine naturale al posto delle perle di destrano.
“Stiamo cercando di utilizzare le biorisorse che rimangono inutilizzate dalla produzione di altre cose o che abbiamo in abbondanza, come alghe e kelp. Poi le usiamo per creare microsfere su cui le cellule possono crescere e che possono poi diventare parte del cibo. Il nostro progetto consiste nel creare microcarrier su cui le cellule possono crescere e nel produrli su larga scala in un grande serbatoio a sospensione agitata”, spiega.
Anche gli avanzi di cibo potrebbero essere utili
Il secondo compito è garantire che le cellule ricevano nutrimento. Oggi vengono spesso alimentate con siero fetale di vitello, ovvero sangue prelevato da vitelli abortiti.
“Se si vuole realizzare un prodotto che non dipenda dall’allevamento, è stupido usare il sangue. Inoltre è costoso, difficile da reperire, ha una qualità variabile e non si può usare negli alimenti. Dobbiamo cercare di trovare risorse che possiamo utilizzare per nutrire quelle cellule in modo da non dover usare quel tipo di siero“, afferma.
Il nutrimento per le cellule è costituito dal liquido in cui le cellule galleggiano e dai microcarrier a cui si attaccano.
“Crediamo che dovremmo essere in grado di realizzare entrambe queste cose a partire da biorisorse disponibili in Norvegia“, afferma Haslene-Hox. Elenca alcune possibilità, come alghe, alghe di mare, materie prime residue di ortaggi e lavorazioni a base vegetale, scarti di altre industrie alimentari come l’allevamento del salmone, gusci d’uovo, pelle e frattaglie di polli e bovini.
Leggi anche:Carne coltivata in laboratorio: più appetibille con nuova tecnica
Gusci d’uovo utili?
Uno dei partner del progetto di ricerca è Norilia, un’azienda che lavora con gusci d’uovo, piume e pelle. La sottile membrana all’interno del guscio d’uovo fa parte del sacco embrionale del pulcino. Supporta la crescita cellulare ed è così efficace che può essere utilizzata anche per favorire la guarigione delle ferite.
“Abbiamo esaminato se le cellule muscolari sono in grado di attaccarsi alle particelle delle membrane dei gusci d’uovo oppure se possiamo mescolarle con l’alginato per far sì che le cellule si attacchino”, afferma.
Finora, i ricercatori hanno trovato alcuni materiali su cui le cellule muscolari sembrano particolarmente a loro agio. Il prossimo passo che intendono compiere è utilizzare le microsfere per ampliare la coltivazione, cosa di cui sono entusiasti.
Haslene-Hox pone alcune domande. “Cosa succede se iniziamo a mescolare questa miscela? Le cellule rimarranno attaccate alla superficie della perla?”