Immagine: il team utilizza la metodologia di recente sviluppo per studiare il cervello dei pazienti con AD a livello di singola cellula. Credito: HKUST.
I ricercatori della Hong Kong University of Science and Technology (HKUST) hanno identificato nuovi bersagli terapeutici per la malattia di Alzheimer (AD) studiando il cervello dei pazienti con una metodologia di nuova concezione. Questo nuovo approccio consente inoltre ai ricercatori di misurare gli effetti di potenziali farmaci sui pazienti con AD, aprendo nuove direzioni per la ricerca e lo sviluppo di farmaci.
Sebbene i meccanismi patologici dell’Alzheimer siano stati studiati per decenni, la malattia rimane incurabile. Uno dei motivi è che gli approcci di ricerca convenzionali hanno una capacità limitata di identificare bersagli molecolari per lo sviluppo di farmaci. L’analisi dei percorsi molecolari e patologici generalmente esamina i cervelli dei pazienti con AD come una singola unità, il che di solito sottostima i contributi di diversi tipi di cellule cerebrali all’AD e qualsiasi anomalia in essi.
Questo è particolarmente il caso di tipi di cellule meno comuni come la microglia (le cellule immunitarie residenti nel cervello ) e le cellule neurovascolari (in particolare le cellule endoteliali), che rappresentano rispettivamente meno del 5% e dell’1% della popolazione totale delle cellule cerebrali.
Vedi anche:Nanozimi per la diagnosi precoce dell’Alzheimer
Tuttavia, un team guidato dalla Prof. Nancy Ip, Vicepresidente per la ricerca e sviluppo, Direttore dello State Key Laboratory of Molecular Neuroscience e Morningside Professor of Life Science presso HKUST, ha più che aggirato questo problema ed ha anche identificato diversi nuovi potenziali bersagli molecolari nelle cellule endoteliali e nella microglia per lo sviluppo di farmaci per l’AD .
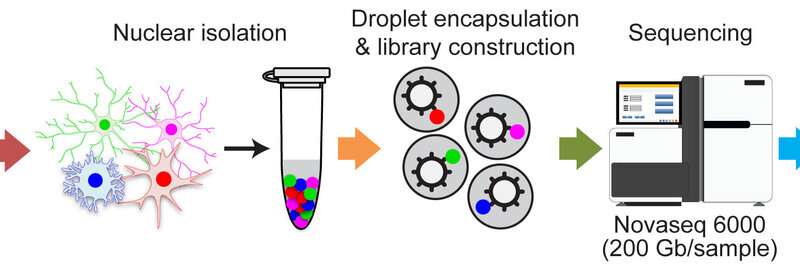
Il team ha esaminato le funzioni di specifici tipi di cellule nel cervello post mortem dei pazienti con AD, che è tipicamente impossibile con approcci convenzionali, utilizzando un’analisi del trascrittoma monocellulare all’avanguardia, che può essere utilizzata per caratterizzare i cambiamenti molecolari nelle singole cellule. Ciò ha prodotto un profilo completo dei cambiamenti specifici del tipo di cellula nel trascrittoma nel cervello dei pazienti con AD. L’analisi successiva ha identificato sottotipi cellulari e percorsi patologici associati all’AD, evidenziando una sottopopolazione specifica di cellule endoteliali presenti nei vasi sanguigni del cervello. Di conseguenza, il team ha scoperto che l’aumento dell’angiogenesi (la formazione di nuovi vasi sanguigni rispetto a quelli attuali) e l’attivazione del sistema immunitario in una sottopopolazione di cellule endoteliali sono associati alla patogenesi dell’AD, suggerendo un legame tra la disregolazione dei vasi sanguigni e l’AD. I ricercatori hanno anche identificato nuovi bersagli per il ripristino dell’omeostasi neurale (la capacità di mantenere uno stato interno relativamente stabile nonostante i cambiamenti esterni) nei pazienti con AD.
Il team ha anche sfruttato l’analisi del trascrittoma monocellulare per studiare il meccanismo con cui la citochina interleuchina-33 (IL-33), un’importante proteina per la segnalazione immunitaria, esercita azioni benefiche, rendendola un possibile intervento terapeutico per l’AD. I ricercatori hanno scoperto che IL-33 riduce la patologia simile all’AD stimolando lo sviluppo di un sottotipo specifico di microglia che aiuta a eliminare la beta-amiloide, una proteina neurotossica che si trova nel cervello di AD. Il team è anche il primo a raccogliere dati sui meccanismi attraverso i quali la microglia si trasforma in uno stato fagocitico che consuma beta-amiloide, che è un importante meccanismo cellulare per la rimozione dei patogeni.
“La composizione cellulare complessa ed eterogenea all’interno del cervello rende difficile studiare i meccanismi della malattia”, ha spiegato il Prof. Ip. “Il progresso della tecnologia unicellulare ci ha permesso di identificare sottotipi cellulari specifici e bersagli molecolari fondamentali per lo sviluppo di nuovi interventi per la malattia di Alzheimer”.
Il team ha recentemente pubblicato il proprio lavoro sulle prestigiose riviste scientifiche Proceedings of the National Academy of Sciences USA (PNAS) e Cell Reports.
Spiegano gli autori:
L’AD, la forma predominante di demenza, colpisce attualmente oltre 50 milioni di individui in tutto il mondo e si prevede che affliggerà 150 milioni di persone entro il 2050. Le sue caratteristiche patologiche includono l’accumulo di depositi extracellulari di beta-amiloide e grovigli neurofibrillari. Nel tempo, l’eliminazione inefficace di questi segni distintivi patologici porta a una disfunzione cellulare nell’AD, con conseguente perdita di memoria, problemi di comunicazione, riduzione delle capacità fisiche e infine morte.